
QbSyst2e.21.html
Système du Québécium
Suivant QbSyst2e.22.html
Précédent QbSyst2e.20.html
Début QbSyst2e.1.html
Suivant annexe QbSyst2e.21bis.html
Chapitre 13
Application à la classification des éléments
Tableaux bidimensionnels nouveaux (suite)

Fig. 273.
Confection de tableaux d'éléments par vêlage.
Au chapitre précédent, nous avons montré comment les tableaux des éléments du système du québécium dérivent de ceux de Mendeleev par pliage et collage. Dans le présent chapitre, nous allons les déduire de la formule du québécium par vêlage (genèse soustractive). Cette formule en tableau, organisée en tenant compte des orbitales est donnée figure 211. Nous reproduisons cette formule en y ajoutant les électrons 119 et 120 afin de remplir toutes les cases de la,grille. Figure 274.
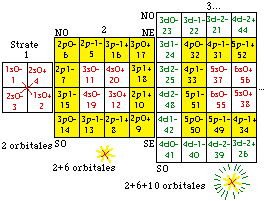
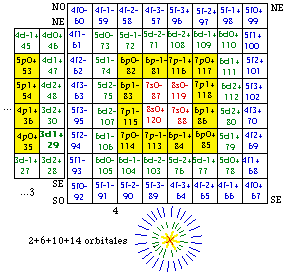
Fig. 274. Formule de Qb 118. 120 cases en couronnes et orbitales, total 60 orbitales. (D'après fig. 211).
Tableau, formule, électron, atome, numéro.
Voici un rappel d'usages linguistiques.
Tout élément ou atome a une formule électronique.
Cette formule peut s'afficher dans un tableau appelé tableau descriptif. Chaque élément réclame un tel tableau affichant sa formule.
Tableau 61. Acceptions de Z.
Z est le numéro atomique d'un élément, égal au nombre d'électrons qu'il contient.
Z est aussi le numéro d'ordre de chacun des électrons dans la formule de cet élément.
Le numéro d'ordre d'un électron avec son caractère est lu dan la formule du québécium.
Z est le numéro d'ordre maximal, soit le plus élevé parmi les numéros d'ordre des électrons dans la formule de cet élément.
ATTENTION. Le symbole Z a donc 3 acceptions. Dans l'ordre ci-dessus, voici des exemples.
Tableau 62. Exemples des 3 acceptions de Z.
Exemple Qb 118.
Z = 118;
Z = 1 à 118;
Z = 118.
Exemple Na 11.
Z = 11;
Z = 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11;
Z = 11.
Exemple Cr 24.
Z = 24;
Z = 1, 2, 3, 4, ... 18,
19, 21, 22, 23, 24, 25;Z = 25.
Dans les exemples de Qb et de Na, 2 lignes sont identiques.
En jouant sur le sens des mots, on peut dire que Na est constitué de H, He, Li, Be, B, C, N, O, F, Ne, en plus de Na. En réalité, Na ne contient pas les 10 autres éléments mentionnés. Il peut les produire par vêlage.
Dans l'exemple de Cr 24, les 3 lignes sont distinctes. Notez l'absence du nombre 20 dans la 2e ligne.
En jouant sur le sens des mots encore, on peut dire que Cr est constitué de H, etc, Cl, A, K, mais non de Ca, Sc, Ti, V. En réalité, Cr ne contient pas les 19 éléments mentionnés en plus de Cr. Il peut les produire par vêlage. Il ne peut pas produire Ca, Sc, Ti, V, parce qu'il est dépourvu de l'électron Z = 20 nécessaire dans la formule de ces 4 atomes, du moins pas par vêlage direct et immédiat.
On peut imaginer qu'il les produirait par un processus de vêlage indirect dans lequel au moins un électron changerait de caractère et de valeur de Z de manière à faire apparaître un électron Z = 20.
Éléments exceptionnels et normaux. Un élément tel que Cr est appelé exceptionnel parce que Z 1re ligne et Z 3e ligne ne sont pas égaux. La plupart des éléments sont normaux et non exceptionnels. Ne pas confondre avec les catégories d'éléments réguliers et non réguliers.
On donne les tableaux descriptifs de Qb 118, Na 11 et Cr 24. On se sert du tableau donnant la formule du québécium figure 211, répété figure 274. Figures 275, 276, 277.
Fig. 275. Tableau descriptif de Qb 118. Toutes valeurs Z de 1 à 118.
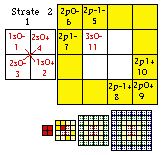
Fig. 276. Tableau descriptif de Na 11. Toutes valeurs Z de 1 à 11.

Fig. 277. Tableau descriptif de Cr 24. Toutes valeurs Z de 1 à 25 sauf 20.
Un tableau des éléments en orbitales. 1re étape.
Nous procédons à partir du tableau donnant la formule de Qb 118, tableau descriptif de cet élément, par genèse soustractive ou vêlage selon les règles 1 et 2 du chapitre 8 :
pour obtenir la formule de l'élément Z, enlever à la formule du québécium tous les électrons de numéro supérieur à Z.
Nous obtenons un tableau descriptif contenant Z cases, celles des électrons de numéros 1 à Z. Il y a autant de tableaux descriptifs que d'éléments. Un exemple pour Z = 11 est donné figure 271. Pour obtenir les éléments 119 et 120 à partir de Qb 118, il faut évidemment une genèse additive, avec addition de 1 ou 2 électrons.
Dans une 1re étape, nous supposons que tous les éléments suivent les règles rappelées ci-dessus et nous apporterons les corrections nécessaire plus tard.
Cela nous évite de confectionner un tableau descriptif pour chacun des éléments. Il nous suffit d'écrire le symbole de l'élément Z dans la case de l'électron Z, et cet élément renferme Z électrons, de 1 à Z. C'est sa formule nominale. Nous convenons qu'un élément occupant la case Z sera désigné par le caractère de l'électron de la même case. Cette convention est à la base de la définition des blocs spdf. Ainsi U 92 est l'élément 4f3.
Voici donc le tableau de tous les éléments, nominalement descriptif de chacun dans cette 1re étape. C'est notre Tableau No 3. Figure 278.
Une case a double sens : elle désigne un élément et un électron. Nous pouvons désigner l'élément par l'électron ou l'électron par l'élément. Dans ce dernier cas, nous sommes portés à dire que l'élément Z contient tous les éléments de 1 à Z-1.
En jouant sur le double sens de Z, nous pouvons dire que chaque élément a son partenaire orbital, celui dont la case est géométriquement opposée à la sienne par rapport à l'origine d'une strate.
Ainsi, C6 et F9, N7 et Ne10.
Orbitales dans les tableaux de Mendeleev.
La géométrie unidimensionnelle des tableaux de Mendeleev, au contraire de celle, bidimensionnelle, de nos tableaux tels que notre No 3, ne met nullement en évidence les partenaires d'une orbitale, exemple C6 et F9, N7 et Ne10 qui sont simplement alignés sur même ligne horizontale dans un bloc p :
B5, C6, N7, O8, F9, F10.
Tableaux No 2 et No 3. Comparaison des géométries.
Les tableaux No 2 et No 3 comptent l'un et l'autre 8 périodes. Leurs strates de même numéro ont le même contenu, ce contenu est remanié en passant d'un tableau à l'autre.
Ce qui est préservé dans le passage No 2 vers No 3 est comme suit : les demiants E et O gardent le même contenu. Les demiants O correspondent à des spins - et les demiants E, à des spins +. La composition des équerres reste la même. Les gaz rares sont placés à l'est de l'axe NS et au voisinage de l'axe OE.
Ce qui change dans ce passage est comme suit : les équerres des quadrants NE et SE sont échangées avec symétrie miroir par rapport à l'axe OE. Les équerres NO et SO subissent une inversion par rapport à leur axe diagonal.
De la sorte, la numérotation des cases dans chaque équerre du tableau No 3 commence au voisinage de l'axe NS.
Un bon exemple pour comprendre ce remaniement est celui de la strate 3.
Le tableau No 2 est commode pour montrer la continuïtè de la numérotation de gauche à droite dans chaque période. Le tableau No 3 est commode pour montrer les orbitales.
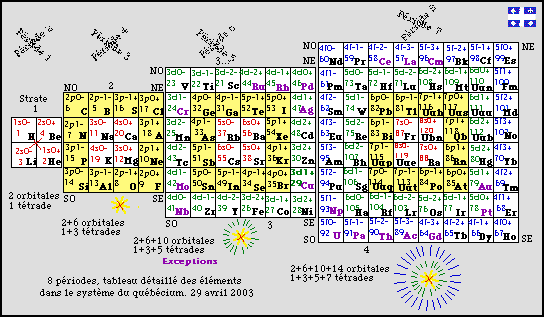
Fig. 278. Tableau des 120 éléments en orbitales 8 périodes. Tableau No 3. La lecture des cases se fait en diagonale par équerres dans les quadrants opposés. Grilles avec des blancs, ouvrez : QbSyst2e.21bis.html.
Ce tableau peut servir de référence. 8 périodes, tableau détaillé des éléments dans le système du québécium.29 avril 2003.
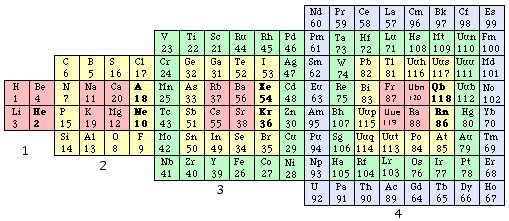
Fig. 279. Tableau No 3 bis. Comme le tableau No 3, mais sans les caractères des électrons.
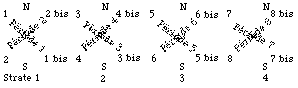
Fig. 280. La lecture des cases se fait en diagonale par équerres dans les quadrants opposés.
La figure 279 donne une version allégée du Tableau No 3, où n'apparaissent pas les caractères des électrons, Tableau No 3bis. Le Tableau No 3bis indique correctement le nombre d'électrons de l'élément.
La figure 279 donne un tableau des éléments pratique, mis en ordre à la manière décrite pour les électrons du québécium figure 211. Il comporte des conventions de lecture identiques à celles du tableau du québécium figure 211. La lecture se fait par équerres consécutives ou quarts de couronnes. Figure 280.
Les périodes ne se trouvent pas en entier d'un côté de l'axe de la figure comme dans le tableau No 2, mais également réparties au nord et au sud.
Tout ce que nous avons dit sur les symétries des cases d'électrons dans le chapitre 9 peut être répété pour les cases d'éléments. Ici, les cases représentent des éléments plutôt que des électrons.
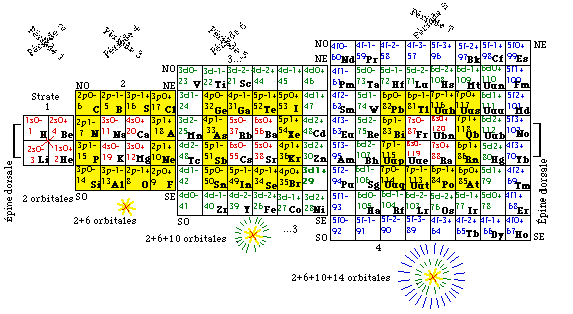
Fig. 281. Les éléments normaux sélection du tableau No 3. Remarquer la colonne vertébrale des 2 rangées centrales.

Fig. 282. Épine dorsale d'éléments normaux. Fins d'équerres et de demi sous-couches. 40 éléments.
La strate 4, strate source.
Par rapport aux strates 3, 2, 1, la strate 4 joue le rôle d'une strate source. Sa structure en termes d'équerres se répète en passant aux strates inférieures. À chaque passage, une couronne extérieure disparaît et les valeurs de n diminuent de 2 unités, les valeurs de l, m, s se répétant.
On constate un parallèle avec le cas des biomolécules. Dans ce cas, la strate 4 joue aussi le rôle d'une strate source par rapport aux strates 3, 2, 1, quoique d'une manière différente.
Un tableau des éléments en orbitales. 2e étape. Éléments normaux et exceptionnels. Épine dorsale.
Le tableau No 4 répète le tableau No 3 en laissant vides les cases des éléments exceptionnels. Il ne contient que les éléments normaux. On peut lire pour chaque élément inscrit sa formule électronique. Ce tableau est un condensé des tableaux figuratifs de ces éléments. Figure 281.
Aux dernières nouvelles, on connaît 19 éléments exceptionnels. Nous comptons comme normaux les éléments peu connus ou restant à découvrir.
Le tableau No 4 manifeste une propriété géométrique remarquable. Les deux rangées centrales de cases sont exemptes d'éléments exceptionnels. Ces rangées renferment les cases terminales des équerres, dans l'ordre des numéros d'ordre croissants des électrons, et chaque équerre renferme une demi sous-couche. Il était déjà connu que ces fins de sous-couches correspondent invariablement à des éléments normaux, mais la mise en évidence de cette particularité se fait tout naturellement dans le tableau 4 de notre système.
C'est l'occasion d'annoncer que l'élément peu connu Z = 102 est normal.
Les éléments exceptionnels. Leurs tableaux figuratifs.
Les 19 éléments exceptionnels se rencontrent uniquement parmi les 58 éléments de transition, situés dans les blocs et couronnes d et f. Ils correspondent aux cases laissées en blanc du tableau No 4. Ces cases sont mises en évidence dans la figure 283.
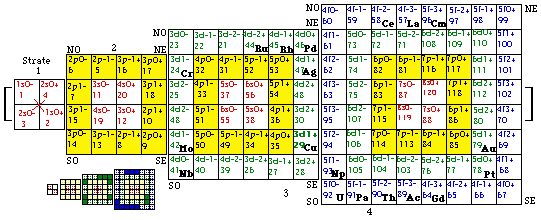
Fig. 283. Les 19 éléments exceptionnels, dans les cases Z qu'ils occuperaient s'ils étaient normaux, dans la figure 281. (Ou dans les cases qu'ils occupent dans le tableau No 3 bis).
Dans cette figure, remarquez les 2 tétrades dessinées par 8 des 19 éléments exceptionnels, comme suit : Cr, Cu, Mo, Ag dans la strate 3 et La, Gd, Ac, Cm dans la strate 4. Les 11 autres ne dessinent pas de tétrades. Les éléments exceptionnels sont traités plus en détail au chapitre suivant.
![]()
Système du Québécium
Suivant QbSyst2e.22.html
Précédent QbSyst2e.20.html
Début QbSyst2e.1.html
Suivant annexe QbSyst2e.21bis.html